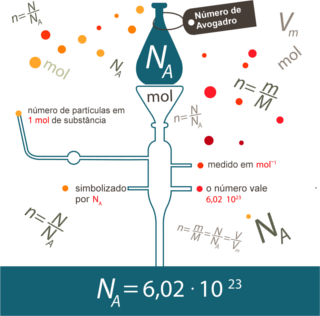
A Lei de Avogadro, também denominada Hipótese de Avogadro, pode ser enunciada da seguinte maneira:
“Volumes iguais, de quaisquer gases, nas mesmas condições de temperatura e pressão, apresentam a mesma quantidade de matéria em mol ou moléculas.”
Mas, como se chegou a essa conclusão? E que volume seria esse?
Bom, conforme foi comprovado pelo cientista Jean Perin, tendo como embasamento os esttudos de Avogadro, determinou, 1 mol de qualquer gás contém 6,02 . 1023 moléculas (Constante de Avogadro ou número de Avogadro). Assim, se 1 mol de qualquer gás contém a mesma quantidade de moléculas, o volume ocupado também será o mesmo, desde que esteja nas mesmas condições de temperatura e pressão.
Quando Avogadro realizou experimentos para determinar quantitativamente esse volume, ele os realizou nas Condições Normais de Temperatura e Pressão (CNTP), em que a temperatura é de 273k e a pressão é de 1 atm. Assim, ele determinou que o volume molar, ou seja, o volume ocupado por um mol de qualquer gás, na CNTP é igual a 22,4L.
Isso significa que, por exemplo, na CNTP, 1 mol de gás hidrogênio ocupa 22,4L e o gás cloro também, mesmo que a massa do gás hidrogênio seja muito menor, pois é de 2 g (H2), enquanto que a massa do gás cloro é de 71g (Cl2).

Esse valor (22,4 L) é muito importante, principalmente em cálculos estequiométricos em que precisamos fazer relações com o volume. Além disso, nas Condições Ambientais de Temperatura e Pressão (CATP), o volume molar passa a ser 25 L
Mas, ainda surge outra pergunta: como pode caber, em um mesmo volume, o mesmo número de moléculas, sendo que existem gases com moléculas maiores e outras menores?
Isso é explicado porque, no estado gasoso, as moléculas estão a uma distância tão grande umas das outras que o tamanho delas é desprezível.