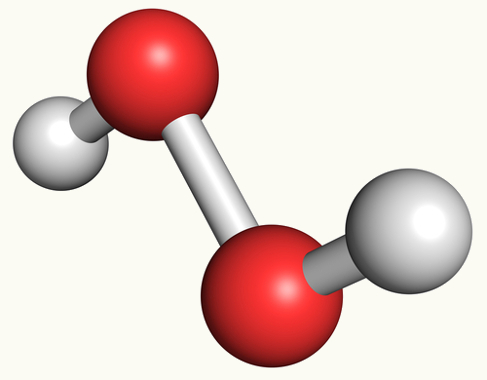
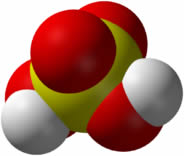
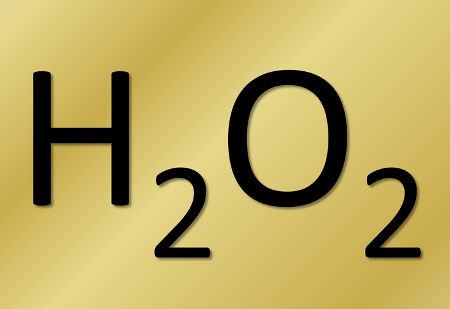Os peróxidos são compostos da função inorgânica dos óxidos (formados por dois elementos e sendo o oxigênio o mais eletronegativo deles) que apresentam em sua estrutura o grupo (O2)2-. O composto mais conhecido desse grupo é o peróxido de hidrogênio, cuja fórmula é dada por H2O2.
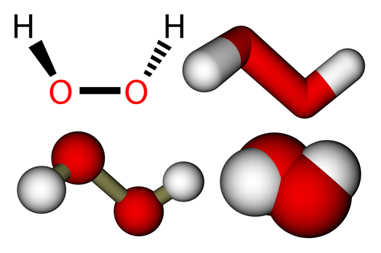
É um líquido incolor, viscoso e instável, que explode violentamente quando aquecido.
Quando se encontra em solução aquosa, o peróxido de hidrogênio é conhecido como água oxigenada (H2O2(aq)). Quando essa solução possui apenas 3% de peróxido de hidrogênio, ela é vendida em supermercados e farmácias para ser utilizada como alvejante ou como antisséptico.
Geralmente a água oxigenada é armazenada em frascos escuros ou opacos, como o mostrado abaixo, pois na presença de luz ela se decompõe.
.jpg)
Sua reação de decomposição é dada por:
2 H2O2(aq) → 2 H2O(l) + O2(g)
A decomposição da água oxigenada é muito mais lenta do que a do peróxido puro.
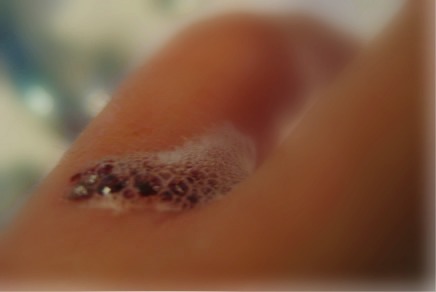
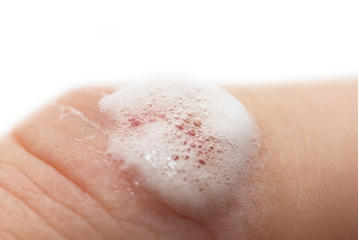
Quando se coloca a água oxigenada sobre um machucado, nota-se imediatamente a formação de uma espuma. Isso acontece porque a água oxigenada está se decompondo, porém, de uma forma bem mais rápida. O nosso sangue possui uma enzima, denominada catalase, que funciona como um catalisador na reação de decomposição da água oxigenada.
Um catalisador é uma substância capaz de acelerar uma reação sem participar dela como um produto, sendo totalmente regenerada no final. O catalisador consegue realizar isso porque ele é capaz de diminuir a energia de ativação de determinadas reações.
A catalase atua dessa maneira na reação de decomposição da água oxigenada. Essa rápida decomposição, gerando gás oxigênio, mata as bactérias anaeróbias, promovendo a assepsia do ferimento.
A batata também possui essa enzima, por isso, se colocarmos um pedaço de batata em um frasco contendo água oxigenada, veremos também a formação de uma espuma, ou seja, ocorrerá um aumento da velocidade dessa reação.
A água oxigenada aplicada em machucados como agente bactericida possui a indicação de 10 volumes. Essa concentração indica que a decomposição do H2O2 presente em 1 litro dessa solução gera 10 litros de gás oxigênio, O2, sob 1 atm e a 0ºC.
Quando essa solução aquosa de peróxido de hidrogênio possui concentrações maiores, por exemplo, 20, 30 e 40 volumes, é usada para descolorir pelos do corpo e cabelos. Soluções com concentrações maiores que 30% são usadas como conservantes em indústrias de alimentos, restauradores de pinturas a óleo, agente oxidante em indústrias, alvejante de madeiras e fibras têxteis e na propulsão de foguetes.