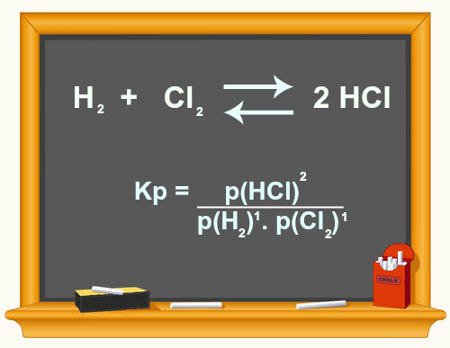
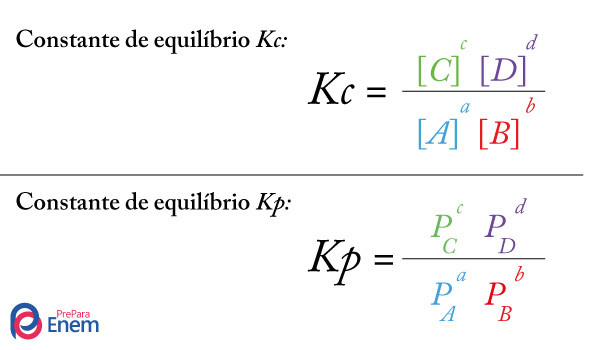No texto “Constantes de Equilíbrio Kc e Kp”, temos todo o estudo teórico sobre essas duas importantes formas de trabalhar um equilíbrio químico. Neste texto, vamos realizar um estudo mais detalhado sobre o cálculo da constante do equilíbrio em termos de pressão (Kp).
Para calcular o Kp, siga estes passos:
1º Passo: Analisar a equação do equilíbrio químico
A constante do equilíbrio em termos de pressão envolve participantes do equilíbrio que estejam no estado gasoso. Por exemplo:
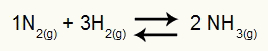
Equação que representa a formação da substância NH3
Os reagentes dessa equação são os gases N2 e H2, e o produto é o gás NH3. Assim, todos os participantes fazem parte da constante de equilíbrio em termos de pressão (Kp).
Já na equação abaixo:

Equação que representa a decomposição da substância CaCO3
O reagente é a substância sólida CaCO3, e o produto é o sólido CaO e o gás CO2. Assim, apenas o CO2 faz parte da constante de equilíbrio em termos de pressão (Kp).
2º Passo: Montar a expressão do Kp para realizar o cálculo
Após analisar a equação da reação em equilíbrio e visualizar se ela apresenta ou não participantes gasosos, podemos montar a expressão que representa a constante do equilíbrio em termos de pressão.
Assim como no Kc (Constante do Equilíbrio em termos de concentração molar), para determinar o Kp, temos a multiplicação das pressões parciais dos produtos no numerador e a multiplicação das pressões parciais dos reagentes no denominador, todos elevados aos seus respectivos expoentes. Por exemplo, no equilíbrio:
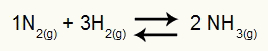
Equação que representa a formação da substância NH3
Nessa equação, temos 2 mol de NH3 no produto e 1 mol de N2 e 3 mol de H2 no reagente. Como todos são gases, temos:
Kp = p(NH3)2
p(N2)1.p(H2)3
3º Passo: Determinar os dados para o cálculo do Kp:
a) Se a pressão parcial for fornecida
Exemplo: (UFES) Em uma dada temperatura, as pressões parciais de cada componente da reação no equilíbrio valem, respectivamente, 0,8 atm, 2,0 atm e 1,0 atm. Qual o valor de Kp?
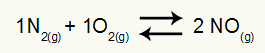
Equação química de formação do monóxido de nitrogênio
a) 1,6
b) 2,65
c) 0,8
d) 0,00625
e) 0,625
Nesse exemplo, temos os valores das pressões parciais de todos os gases participantes do equilíbrio:
-
Pressão parcial do NO no equilíbrio: 1,0 atm
-
Pressão parcial do N2 no equilíbrio: 0,8 atm
-
Pressão parcial do O2 no equilíbrio: 2,0 atm
Como os valores são do equilíbrio, basta utilizá-los na expressão do Kp:
Kp = p(NO)2
p(N2)1.p(O2)1
Kp = (1)2
(0,8)1.(2)1
Kp = 1
0,8 . 2
Kp = 1
1,6
Kp = 0,625
OBS.: Note que o resultado do Kp é adimensional, ou seja, não tem unidade. Isso ocorre porque temos o atm elevado a dois no numerador e atm multiplicando atm no denominador. Resumindo: ao cortar, não sobra nenhum atm.

Determinação da unidade do Kp
b) Se forem fornecidas a pressão total e as pressões parciais de alguns componentes do equilíbrio
Exemplo: (Cesesp-PE) Para a reação
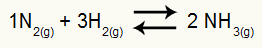
Equação química de formação da amônia
as pressões parciais de H2 e N2 no equilíbrio são, respectivamente, 0,400 e 0,800 atm. A pressão total do sistema é 2,80 atm. Qual é o valor de Kp?
Nesse exemplo, temos:
-
Pressão parcial do H2 no equilíbrio: 0,4 atm
-
Pressão parcial do N2 no equilíbrio: 0,8 atm
-
Pressão total do sistema no equilíbrio: 2,8 atm
Antes de iniciar o cálculo, devemos determinar a pressão parcial do NH3. Devemos lembrar que a pressão total do sistema é a soma das pressões parciais dos gases dentro dele:
- Para o NH3
pt = p(H2) + p(N2) + p(NH3)
2,8 = 0,4 + 0,8 + p(NH3)
p(NH3) = 2,8 – 0,4 – 0,8
p(NH3) = 1,6 atm
Por fim, basta utilizar os valores encontrados na expressão do Kp do processo:
Kp = p(NH3)2
p(H2)3.p(N2)1
Kp = (1,6)2
(0,4)3.(0,8)1
Kp = 2,56
0,064.0.8
Kp = 2,56
0,0512
Kp = 50 atm-2
OBS.: A unidade é atm-2 porque temos o atm elevado a dois no numerador e atm elevado a três multiplicando outro atm no denominador. Resumindo: ao cortar, sobram dois atm no denominador, o que o deixa com expoente negativo.
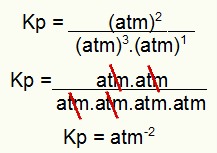
Determinação da unidade do Kp do exercício
c) Se forem fornecidas a pressão do sistema e a porcentagem de um dos componentes do equilíbrio
Exemplo: (Usina-SP) Quando é alcançado o equilíbrio:

Equação que representa o equilíbrio químico entre NO2 e N2O4
a pressão é 2 atm e há 50% de NO2 em volume. O valor da constante de equilíbrio em pressões parciais (Kp) deve ser:
a) 0,2 atm-1
b) 0,25 atm-1
c) 1 atm-1
d) 0,5 atm-1
e) 0,75 atm-1
Nesse exemplo, o enunciado informa a pressão total e diz que existe 50% de NO2 quando o equilíbrio é alcançado. Inicialmente vamos determinar a pressão parcial do NO2:
- Para o NO2
Basta multiplicar a pressão total pela porcentagem de NO2 no equilíbrio:
P(NO2) = 2.0,5
P (NO2) = 1 atm
Em seguida, determinamos a pressão do N2O4 sabendo que a pressão total do sistema é a soma das pressões parciais dos gases:
- Para o N2O4
pt = p(N2O4) + p(NO2)
2 = p(N2O4) + 1
p(N2O4) = 2-1
p(N2O4) = 1 atm
Por fim, basta utilizar os valores encontrados na expressão do Kp do processo:
Kp = p(N2O4)1
p(NO2)2
Kp = (1)1
(1)2
Kp = 1 atm-1
OBS.: A unidade é atm-1 porque temos o atm elevado a um no numerador e o atm elevado a dois no denominador. Resumindo: ao cortar, sobra um atm no denominador, o que o deixa com expoente negativo.
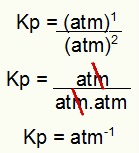
Determinação da unidade do Kp do exemplo
d) Se forem fornecidas a pressão total do sistema e as frações molares (frações em quantidade de matéria) dos seus participantes
Exemplo: (UFU) Calcular a constante de equilíbrio kp da reação:
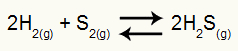
Equação química de formação do Sulfeto de Hidrogênio
A 750oC, sabendo-se que o sistema em equilíbrio encontra-se a pressão de 15 atm e sendo as frações em quantidade de matéria dos constituintes:
H2 = 1/6
S2 = 1/3
H2S = 1/2
a) 27 atm-1
b) 36 atm-1
c) 9 atm-1
d) 15 atm-1
e) 1,8 atm-1
Como o enunciado forneceu a pressão total e a fração molar de cada participante, inicialmente devemos determinar a pressão parcial dos participantes multiplicando sua fração pela pressão total:
- Para o H2:
p(H2) = 1 .15
6
p(H2) = 2,5 atm
- Para o S2:
p(S2) = 1 .15
3
p(S2) = 5 atm
- Para o H2S:
p(H2S) = 1 .15
2
p(S2) = 7,5 atm
Em seguida, basta utilizar os valores encontrados na expressão do Kp do processo:
Kp = p(H2S)2
p(H2)2.p(S2)1
Kp = (7,5)2
(2,5)2. (5)1
Kp = 56,25
6,25 . 5
Kp = 56,25
31,25
Kp = 1,8 atm-1
OBS.: A unidade é atm-1 porque temos o atm elevado a um no numerador e o atm elevado a dois no denominador. Resumindo: ao cortar, sobra um atm no denominador, o que o deixa com expoente negativo.
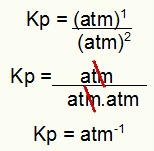
Determinando a unidade do Kp do exemplo