Para determinar o pH de uma solução-tampão, é importante conhecer a característica da solução com a qual se está lidando. Uma solução-tampão pode ser classificada em:
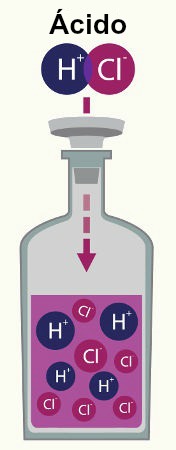
a) Solução-tampão ácida
É formada por um ácido fraco (Clique aqui e saiba sobre a classificação dos ácidos quanto à força) e por um sal que apresente o mesmo ânion do ácido. Um exemplo é a mistura formada pelo ácido cianídrico (HCN) e o sal cianeto de sódio (NaCN).
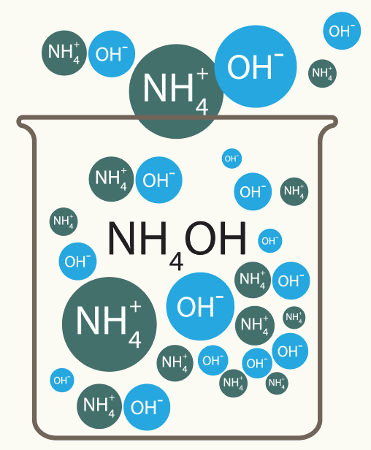
b) Solução-tampão básica
É a solução-tampão formada por uma base fraca (Clique aqui e saiba sobre a classificação das bases quanto à força) e por um sal que apresente o mesmo cátion da base. Um exemplo é a mistura formada pelo hidróxido de amônio (NH4OH) e o sal cloreto de amônio (NH4Cl).
Fórmulas para cálculo do pH de uma solução-tampão
-
Para solução-tampão ácida:
Para determinar o pH de uma solução-tampão ácida, basta somar o valor do pKa do ácido com o logaritmo da relação entre a concentração molar do sal e a concentração molar do ácido:
pH = pKa + log [sal]
[ácido]
OBS.: Caso o exercício não forneça o valor do pKa, para determiná-lo, basta calcular o logaritmo do Ka (constante de ionização do ácido):
pKa = -log [Ka]
-
Para solução-tampão básica
Para determinar o pH de uma solução-tampão básica, basta somar o valor do pKb da base com o logaritmo da relação entre a concentração molar do sal e a concentração molar da base:
pH = pKb + log [sal]
[base]
OBS.: Caso o exercício não forneça o valor do pKa, para determiná-lo, basta calcular o logaritmo do Kb (constante de dissociação da base):
pKb = -log [Kb]
Para uma solução básica, podemos ainda utilizar a seguinte fórmula (caso o exercício forneça ou faça referência ao pKw):
pH = pKw - pKb - log [sal]
[base]
Exemplos de cálculo do pH de uma solução-tampão
Exemplo 1: (UNIFOR-CE) Ácido láctico – CH3CH(OH)COOH – e lactato de sódio – CH3CH(OH)COONa - formam, em água, uma solução-tampão. Tal solução contendo 0,12 mol/L do ácido e 0,10 mol/L do lactato tem, a 25 ºC, pH bem definido. Para calcular seu valor, utilizou-se o valor da constante de equilíbrio, a 25 ºC, de:
![]()
Keq = 1,4.10-4 mol/L
Considerando-se que a constante de equilíbrio é muito pequena, ou seja, forma-se quantidade desprezível de lactato proveniente do ácido, pode-se calcular o pH da solução. Seu valor encontra-se no intervalo
a) 1 – 3
b) 3 – 4
c) 4 – 5
d) 5 – 6
e) 7 – 9
Resolução:
Dados fornecidos pelo exercício:
-
[CH3CH(OH)COOH] = 0,12 mol.L–1
-
[CH3CH(OH)COONa] = 0,10 mol.L–1
-
Ka = 1,4.10-4
-
pH = ?
Inicialmente temos que encontrar o valor do pKa, já que o exercício forneceu o valor do Ka por meio da seguinte expressão:
pKa = -log [Ka]
pKa = -log 1,4.10-4
pKa = 4. log 10 – log 1,4
pKa = 4.1 – 0,146
pKa = 4 – 0,146
pKa = 3,85
Como se trata de uma solução-tampão ácida e temos diversos dados, basta utilizá-los na expressão a seguir:
pH = pKa + log [sal]
[ácido]
pH = 3,85 + log 0,10
0,12
pH = 3,85 + log 0,83
pH = 3,85 – 0,080
pH = 3,77
Exemplo 2: Qual é o pH aproximado de uma solução obtida pela mistura de 100 mL de uma solução aquosa de NH4OH 1 x 10–2 mol.L–1 e 100 mL de uma solução aquosa de NH4Cl 5 x 10–2 mol.L–1, sabendo-se que o Kb do NH4OH é 4,9 x 10–10 (pKb = 9,31)? (Dados: log 5 = 0,7)
a) pH = 2
b) pH = 12
c) pH = 10
d) pH = 7
e) pH = 4
Resolução:
Dados fornecidos pelo exercício:
-
[NH4OH] = 1 x 10–2 mol.L–1
-
[NH4Cl] = 5 x 10–2 mol.L–1
-
Kb = 4,9 x 10–10
-
pKb = 9,31
-
log 5 = 0,7
-
pH = ?
Como se trata de uma solução-tampão ácido (formado por uma base fraca e um sal com um ânion que origina ácido forte) e temos diversos dados, inicialmente devemos utilizar a expressão abaixo para determinar o pOH:
pOH = pKb + log [sal]
[base]
pOH = 9,31 + log 5.10-2
1.10-2
pOH = 9,31 + log 5
pOH = 9,31 + 0,7
pOH = 10
Em seguida, utilizamos a expressão abaiixo para determinar o valor do pH:
pH + pOH = 14
pH + 10 + 4
pH = 14 - 10
pH = 4
Videoaula relacionada: