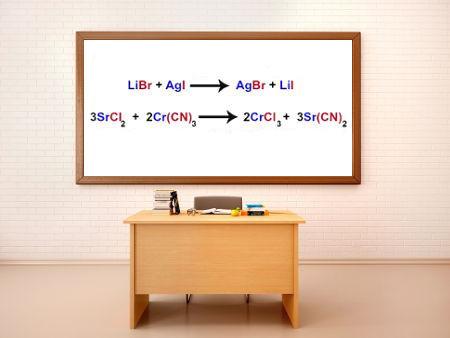
Os sais são derivados de reações entre ácidos e bases, que são chamadas de reações de neutralização. O ânion do sal se une ao cátion da base, podendo formar diferentes tipos de sais. Essas reações de neutralização podem ser totais ou parciais e, dependendo de qual ocorrer, o sal formado também será distinto.
Além disso, existem alguns sais que apresentam moléculas de água em seus retículos cristalinos, produzindo outro tipo de sal.
De acordo com esses critérios, podem-se formar seis tipos de sais diferentes, que são: sal neutro, sal básico (hidroxissal), sal ácido (hidrogenossal), sal duplo (misto), sal hidratado e alúmen. Veja cada um:
1. Sal Neutro: O sal e a base que o originaram são ambos fortes ou ambos fracos e, desse modo, possuem apenas um cátion e um ânion, que são, respectivamente, diferentes do H+ e do OH-. São chamados de neutros porque não alteram o pH da água quando adicionados à ela, sendo que eles não sofrem hidrólise;
Exemplos:
- NaCl:
Cátion → Na+ (vem do hidróxido de sódio, NaOH, uma base forte);
Ânion → Cl- (vem do ácido clorídrico, HCl, um ácido forte).
.jpg)
- NH4CN:
Cátion → NH42+ (vem do hidróxido de amônio, NH4OH, uma base fraca);
Ânion → CO3-2 (vem do ácido cianídrico, HCN, um ácido fraco).
2. Sal Básico ou Hidroxissal: É proveniente de uma reação entre uma base forte e um ácido fraco, assim, quando adicionado à água, produzirá ânions hidroxila (OH-), tornando o meio básico (pH > 7);
Exemplo:
- NaOOCCH3:
Cátion → Na+ (vem do hidróxido de sódio, NaOH, uma base forte);
Ânion → CH3COO–(vem do ácido etanoico, CH3COOH, H2CO3, um ácido fraco).
No exemplo acima, o ânion acetato (CH3COO–) se hidrolisa em meio aquoso e forma o ácido acético e íons hidroxila (OH–), tornando a solução básica.
3. Sal Ácido ou Hidrogenossal: É proveniente de uma reação entre um ácido forte e uma base fraca, assim, quando adicionado à água, produzirá cátion hidrogênio (H+), tornando o meio ácido (pH < 7);
Exemplo:
- NH4Cl(s):
Cátion → NH42+ (vem do hidróxido de amônio, NH4OH, uma base fraca);
Ânion → Cl- (vem do ácido clorídrico, HCl, um ácido forte).
Quando o sal acima é adicionado à água, o seu cátion oriundo de uma base fraca sofre hidrólise e gera íons H3O+ (aq), tornando a solução ácida.
4. Sal Misto ou Duplo: É proveniente de uma reação de neutralização parcial, pois o sal possuirá dois cátions, sendo que nenhum deles pode ser o H+, ou possuirá dois ânions, em que nenhum deles é o OH-;
Exemplos:
- KNaSO4: cátions →K+ e Na+; ânion → SO42-
- CaClBr: cátion → Ca+; ânions → Cl- e Br-
5. Sal Hidratado: Alguns sais são higroscópicos, ou seja, capazes de absorver facilmente a água do ambiente. Essas moléculas de água em proporções definidas passam a ficar no retículo cristalino do sal no estado sólido;
Exemplos: CuSO4 . 5 H2O = sulfato de cobre II penta-hidratado
Esse sal hidratado possui coloração azul quando hidratado, mas ao ser aquecido e perder suas moléculas de água, ele se torna o sulfato de cobre II anidro, que tem coloração branca.

Essa mudança de cor também ocorre no caso do cloreto de cobalto II que, quando está hidratado, é da cor rosa, mas quando está anidro, é da cor azul. É esse sal que é usado naqueles galos do tempo que indicam se o tempo vai permanecer seco ou se provavelmente irá chover. Leia sobre isso no texto Equilíbrio Químico na Previsão do Tempo.
6. Alúmen: São sais formados por dois cátions, sendo um monovalente (com carga +1) e o outro trivalente (com carga +3), por um único ânion (o sulfato (SO42-)) e por água de cristalização.
Exemplo: KAl(SO4)2 . 12 H2O = sulfato de potássio e alumínio dodeca-hidratado (conhecido popularmente como pedra-ume).
Aproveite para conferir a nossa videoaula relacionada ao assunto: