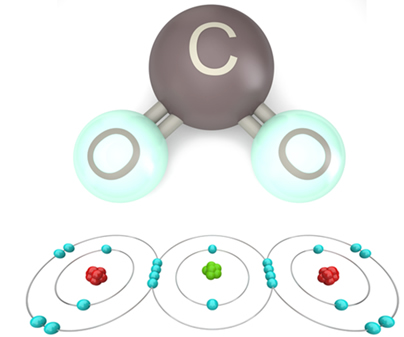
As substâncias moleculares são formadas pela união de átomos de elementos que precisam receber elétrons para ficarem estáveis, formando uma ligação química em que compartilham pares de elétrons (ligação covalente).
Isso ocorre com base na Regra do Octeto, cuja ideia foi enunciada pela primeira vez em 1916, pelo químico alemão Walther Kossel (1888-1956), sendo chamada de teoria eletrônica de valência. Mais tarde, ela foi aperfeiçoada de maneira independente pelos químicos norte-americanos Gilbert Lewis (1875-1946) e Irving Langmuir (1881-1957).
Essa teoria baseia-se no fato de que os únicos elementos cujos átomos apresentam-se isolados de forma estável na natureza são os gases nobres (família 18 ou VIII A). Todos esses elementos possuem oito elétrons na última camada eletrônica (camada de valência) ou dois elétrons (no caso do hélio que possui apenas a primeira camada (K)).
Assim, estabeleceu-se que os átomos de diferentes elementos fazem ligações químicas com a finalidade de ficarem com a configuração eletrônica de um gás nobre e, dessa forma, tornarem-se estáveis.
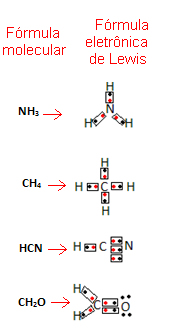
Gilbert N. Lewis propôs, então, uma forma de representar essas ligações que se estabeleciam nas moléculas, que ficou conhecida como Fórmula Eletrônica de Lewis.
Essa fórmula é importante porque ela não só mostra os elementos e o número de átomos envolvidos, mas também os elétrons da camada de valência de cada átomo e quantos pares eletrônicos são compartilhados por cada átomo.
Os elétrons da camada de valência são representados por bolinhas ou x e são colocados em volta do símbolo do elemento químico. Os elétrons compartilhados são colocados lado a lado:
.jpg)
Vamos dar alguns exemplos de como é escrita essa fórmula:
- A fórmula molecular do gás hidrogênio é H2. O hidrogênio está na família IA da tabela periódica porque ele possui apenas um elétron na sua camada de valência. Assim, cada átomo de hidrogênio é representado com uma “bolinha” ao seu redor: H? ?H.
Segundo a regra do octeto, visto que possui somente a camada K, ele precisa receber mais um elétron para ficar com dois elétrons na camada de valência e ficar estável. Desse modo, esses dois átomos de hidrogênio compartilham um par de elétrons, ficando ambos estáveis, e sua fórmula eletrônica é a seguinte:
![]()
- Seguindo o mesmo raciocínio, vamos escrever a fórmula molecular do gás oxigênio (O2), do gás nitrogênio (N2) e do cloro (C?2), todos sendo substâncias simples:

- Agora veja alguns exemplos de substâncias compostas:
Videoaula relacionada: