Todos os anos a sociedade sofre um enorme prejuízo econômico e ambiental devido às corrosões dos metais, em especial do aço. Estudos mostram que só nos Estados Unidos o gasto anual para cobrir os prejuízos causados pela corrosão é de 80 bilhões de dólares.
A corrosão é a oxidação do metal por agentes naturais, principalmente o oxigênio e a água. Ela traz prejuízos econômicos porque a vida útil dos objetos metálicos, tais como tubulações, estruturas de construções, edifícios, pontes, viadutos, instalações industriais, máquinas, entre outros, reduz-se drasticamente, sendo necessário produzir mais desses metais.
Esse fenômeno também coloca em risco a vida das pessoas, pois a corrosão de equipamentos importantes pode levar a acidentes e contaminações.
Além disso, traz prejuízos para o meio ambiente, pois o processo de produção do aço envolve a exploração de minérios e grandes gastos de energia para reduzir os óxidos de ferro nos fornos siderúrgicos.

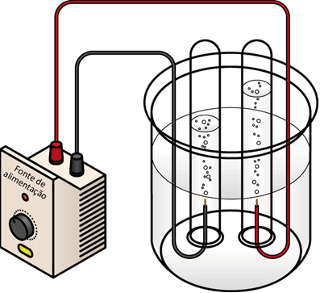
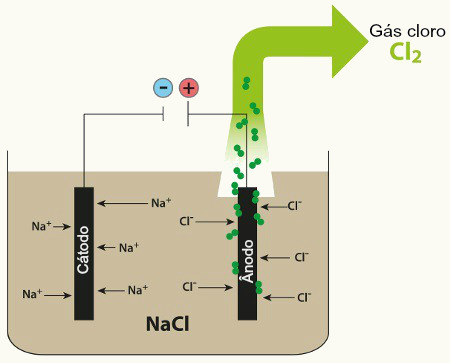
Assim, para minimizar esses prejuízos, procura-se realizar a proteção dos metais para evitar sua corrosão. No caso do aço, uma das técnicas utilizadas é a galvanização. Nesse processo, o aço é revestido de zinco e representa uma proteção catódica. Esse revestimento pode se dar de duas formas: mergulhando-se a peça no zinco fundido, como é mostrado na ilustração logo mais abaixo, ou por eletrodeposição do metal. Esse último processo é bem explicado no texto Galvanoplastia. Nesse texto é mostrado que por meio de um processo de eletrólise é possível revestir um metal colocado no cátodo com outro metal mais nobre, que pode ser colocado no ânodo ou na solução aquosa. Assim, quando esse processo é feito usando o zinco para revestir a peça metálica, a galvanoplastia se torna uma galvanização.

Para entender o princípio de funcionamento da galvanização, vejamos primeiro o que faz o aço enferrujar.
O aço é uma liga metálica composta em sua maioria de ferro (composição do aço = Fe (≈98,5%), C (0,5 a 1,7%), Si, S e O (traços)). O ferro tem menor potencial de redução do que o oxigênio e, portanto, ele sofre oxidação:
Fe (s) → Fe2+ + 2e-
Acontecem várias reações de redução, dependendo das condições, mas as principais que levam à formação da ferrugem são as da água e do oxigênio:
O2 + 2 H2O + 4 e- → 4 OH-
Como já dito, o oxigênio tem maior potencial de redução que o ferro, portanto, ele irá ser o cátodo e o ferro, o ânodo:
Ânodo: 2 Fe (s) → 2Fe2+ + 4e-
Cátodo: O2 + 2 H2O + 4e- → 4 OH-____
Reação global: 2 Fe + O2 + 2 H2O → 2 Fe (OH)2
Posteriormente, o hidróxido de ferro (II), Fe (OH)2, é oxidado a hidróxido de ferro (III), Fe (OH)3, devido àpresença do oxigênio:
4 Fe (OH)2 + O2 + 2 H2O → 4 Fe (OH)3
Esse hidróxido pode perder água e se transformar no óxido de ferro (III) mono-hidratado, que possui cor castanho-avermelhada, ou seja, é a ferrugem:
2 Fe (OH)3 → Fe2O3 . H2O + 2 H2O
A ferrugem se solta facilmente e isso acelera o processo de corrosão, porque a superfície metálica fica em contato com o oxigênio do ar.
Assim, no caso da galvanização, o zinco metálico do qual o aço é revestido é melhor agente redutor do que o ferro, pois enquanto o seu potencial de redução é igual a – 0,76 V, o do ferro é igual a -0,44 V. Veja que o potencial de redução do zinco é menor, em consequência, o seu potencial de oxidação é maior e é ele que vai oxidar, e não o ferro.
Dessa forma, o zinco atua como um metal de sacrifício, pois ele irá oxidar no lugar do ferro, mantendo a estrutura metálica intacta.
Além disso, a corrosão do zinco é mais lenta do que a do ferro, isso porque na medida em que ele vai sendo corroído, vai se formando uma película de Zn(OH)2, que ao contrário da ferrugem, não se solta facilmente do metal, pois ela é bem aderente e praticamente insolúvel em água.
Mas, e se o objeto for riscado, deixando o ferro em contato com o ar?Não há preocupação, porque apesar do ferro se oxidar, o zinco também se oxida e os íons Fe2+ que foram formados na oxidação são reduzidos a ferro metálico (Fe). Além disso, a película de Zn(OH)2 se deposita sobre o ferro exposto e a peça fica novamente protegida.