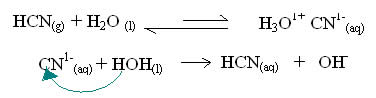| Hidrólise salina é o processo em que um íon proveniente de um sal reage com a água. |
Todos os sais dissolvidos na água sofrem dissociação, liberando seus íons, conforme a reação genérica abaixo, onde x e y representam os menores números inteiros não divisíveis:
Sal + água → cátion + ânion
CxAy(s) + x.y H2O(l) →x C+y(aq) + yA-x (aq)
No entanto, conforme dito no início, alguns desses cátions ou ânions reagem com a água, originando o que denominamos de hidrólise. Assim, soluções ácidas e básicas com diferentes valores de pH podem ser obtidas.
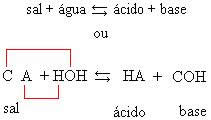
É importante lembrar que:
| Somente sais derivados de ácidos e bases fracos reagem com água. |
Não ocorre hidrólise de sais derivados de ácidos fortes e bases fortes. Nesse caso, a solução formada será neutra, ou seja, com pH= 7. Se uma base forte entrar em contato com a água, ela permanecerá predominantemente dissociada e um ácido forte predominantemente ionizado. Isso nos mostra que praticamente não há afinidade entre seus íons e os íons formados pela água. Vejamos melhor essa questão:
O grau de ionização (α) é que define se um ácido ou base são fracos, moderados ou fortes, conforme a regra a seguir:
*Para ácidos:
α > 50% - ácido forte (exemplos: ácido clorídrico (HCl), ácido nítrico (HNO3) e ácido sulfúrico (H2SO4));
5%< α < 50%- ácido semiforte (exemplos: ácido sulfuroso (H2SO3), ácido fosfórico (H2PO4) e ácido fluorídrico (HF));
α < 5% - ácido fraco (exemplos: ácido sulfídrico (H2S), ácido bórico (H3BO3) e ácido cianídrico (HCN)).
*Para bases:
α ≈100% - bases fortes: bases de metais alcalinos (exemplos: hidróxido de sódio (NaOH) e hidróxido de potássio (KOH)) e algumas de metais alcalino-terrosos (exemplos: hidróxido de cálcio (Ca (OH) 2) e hidróxido de estrôncio (Sr(OH)2);
α < 5% - bases fracas: bases de metais de transição e dos metais das famílias 13, 14 e 15 (exemplos: hidróxido de magnésio (Mg(OH)2) e hidróxido de amônio (NH4OH)).
*O cátion só reage com a água se formar uma base fraca: O grau de afinidade do cátion desse sal pelo íon hidróxido (OH-) fornecido pela autoionização da água deve ser grande. Isto é visto pelo fato de uma base fraca entrar em contato com a água e observarmos que ela se mantém predominantemente na forma agregada.
Exemplo: no hidróxido de amônio, uma base fraca, o cátion formado (NH41+) tem grande afinidade com o íon OH- e reage com a água:
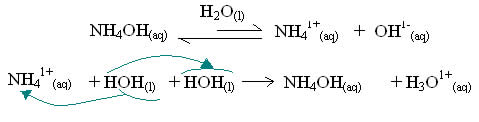
*O ânion só reage com a água se formar um ácido fraco: O grau de afinidade do ânion formado pelo sal na água tem que ser grande pelo próton H+. O ácido fraco ao entrar em contato com a água permanece predominantemente na forma molecular:
Exemplo: o ácido cianídrico, HCN, é um ácido fraco. Seus ânions (CN-) têm grande afinidade com o próton H+.