Denominam-se leis da radioatividade as conclusões propostas pelo químico inglês Frederick Soddy no ano de 1911, ao observar o comportamento dos átomos emde radiação alfa e beta.
De acordo com Soddy, sempre que um átomo emitir uma radiação alfa ou beta, ele originará um novo núcleo, que dependerá do tipo de radiação emitida:
-
Radiação alfa: formada por dois prótons e dois nêutrons;
-
Radiação beta: não é composta por prótons nem nêutrons, mas por um elétron.
Primeira lei da radioatividade
A primeira lei da radioatividade, segundo Soddy, está relacionada com a emissão de partícula alfa a partir do núcleo de um átomo instável, que resultará em:
-
Formação de um novo elemento químico;
-
Esse elemento apresentará um número de massa quatro unidades menor que o átomo original;
-
Seu número atômico passará a ter duas unidades a menos que o átomo de origem.
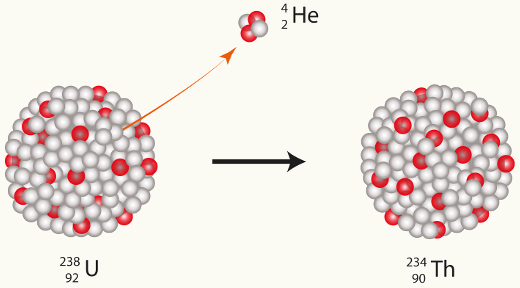
Representação esquemática da primeira lei da radioatividade
Essa lei pode ser representada pela seguinte equação química:
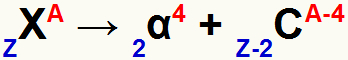
Equação geral de formação de um novo átomo de acordo com a primeira lei da radioatividade
A segunda lei da radioatividade relaciona-se com a emissão de partícula beta pelo núcleo de um átomo instável, que resultará na:
-
Formação de um novo elemento químico;
-
Esse novo elemento apresentará mesmo número de massa do átomo de origem;
-
Seu número atômico terá uma unidade a mais em relação ao átomo de origem.
.jpg)
Representação esquemática da segunda lei da radioatividade
Essa lei é representada pela seguinte equação química:
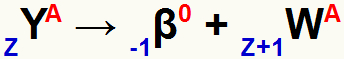
Equação geral que representa a formação de um novo átomo de acordo coma segunda lei da radioatividade
O número atômico do novo átomo aumenta em uma unidade porque, de acordo com a hipótese de Fermi, um nêutron sofre uma transformação, o que resultará na formação de um elétron (radiação beta), um próton e um neutrino ou antineutrino.
Exemplos de aplicação das leis da radioatividade
1º Exemplo: Emissão alfa a partir de um átomo de urânio (92U234).
De acordo com a primeira lei, ao emitir partícula alfa, o urânio formará um novo elemento:
-
Com número de massa menor que a do urânio em quatro unidades, isto é, igual a 230;
-
Com número atômico menor em duas unidades, ou seja, igual a 90.
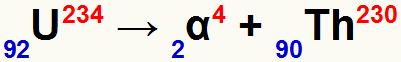
Aplicação da primeira lei da radioatividade com o urânio
2º Exemplo: Emissão alfa a partir de um átomo de carbono (6C14).
Segundo a segunda lei, ao emitir partícula beta, o carbono formará um novo elemento:
-
Com número de massa igual ao do carbono (14);
-
Com um número atômico uma unidade maior que o do carbono, que ficará igual a 7.
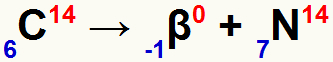
Aplicação da segunda lei da radioatividade com o carbono
*Créditos da imagem: Catwalker/shutterstock
Aproveite para conferir nossa videoaula relacionada ao assunto: