As ligações covalentes acontecem sempre entre átomos de hidrogênio, entre ametais ou entre um ametal e um hidrogênio. Quando ocorrem, são representadas por:
-
ligação simples (?): representa uma ligação que é chamada de sigma (σ);
-
ligação dupla (=): representa duas ligações, sendo um sigma (σ) e uma pi (π);
-
ligação tripla (≡): representa três ligações, sendo uma sigma e duas pi (π).
Uma ligação covalente acontece quando um orbital incompleto (possui um único elétron) de um átomo interpenetra no orbital incompleto de outro átomo. A ligação pi ocorre especificamente quando um orbital p interpenetra outro orbital p no eixo paralelo.
Veja um exemplo na molécula de N2 (gás nitrogênio):
N ≡ N
Podemos afirmar que dois orbitais incompletos de ambos os átomos de nitrogênio interpenetraram-se no eixo paralelo porque, nessa molécula (N2), temos uma ligação tripla, na qual uma das ligações é sigma e as outras duas ligações são do tipo pi. Para comprovar, basta pegar o número atômico (sete elétrons) do nitrogênio e fazer a sua distribuição eletrônica:
1s2
2s2 2p3
Observando a sua distribuição eletrônica, percebemos que, no subnível p do segundo nível (2p), o nitrogênio apresenta três orbitais incompletos:

Os três orbitais atômicos incompletos do subnível p do nitrogênio
Como os orbitais p estão incompletos, o desenho esquemático para eles é:

Os orbitais p sempre são representados por hélices
Como a ligação pi ocorre entre orbitais paralelos, considerando os dois nitrogênios envolvidos na molécula do N2 , podemos perceber quais são esses orbitais (vermelhos e azuis):
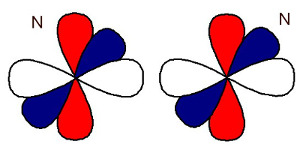
Orbitais dos átomos de nitrogênio que formam o N2
Observação: os dois orbitais em branco realizam uma interpenetração no mesmo eixo, sendo responsáveis pela ligação sigma.
A representação da ligação pi entre esses dois átomos de nitrogênio ocorre por meio de arcos (negros) feitos entre os dois orbitais verticais (vermelhos) e os dois diagonais (azuis) da seguinte forma:
.jpg)
Representação das ligações pi presentes em uma molécula de N2







