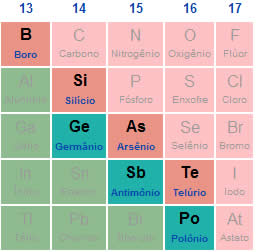
Denominam-se de metais nobres todos os elementos químicos metálicos (aqueles que são capazes de perder elétrons e transformar-se em cátions) que apresentam uma baixíssima reatividade quando comparados com qualquer outro metal da Tabela Periódica.
São metais nobres os seguintes elementos químicos:
-
Ouro (representado pela sigla Au)
-
Prata (representada pela sigla Ag)
-
Paládio (representado pela sigla Pd)
-
Platina (representada pela sigla Pt)
-
Mercúrio (representado pela sigla Hg)
-
Cobre (representado pela sigla Cu)
Como os metais nobres apresentam baixa reatividade, ou seja, apresentam dificuldade de perder elétrons, são elementos químicos que possuem uma baixa eletropositividade.
Assim, um metal dito nobre não tem a mesma capacidade do Ferro, por exemplo, de sofrer o fenômeno da oxidação. Assim, apresenta uma maior durabilidade em comparação com os outros metais. Essa baixa reatividade faz dos metais nobres os principais constituintes de joias, por exemplo.
Vamos conhecer agora mais detalhadamente esses elementos químicos:
Posição na Tabela Periódica
De uma forma geral, os metais nobres são elementos que pertencem às famílias B, sendo, portanto, considerados elementos de transição. Veja a posição de cada um:
-
Ouro: 6º período da família IB
-
Prata: 5º período da família IB
-
Mercúrio: 6º período da família IIB
-
Platina: 6º período da família VIIIB (ou grupo 10)
-
Paládio: 5º período da família VIIIB (ou grupo 10)
-
Cobre: 1º período da família IB
De forma mais específica, são denominados de elementos de transição externa, pois todos eles apresentam o subnível d como o mais energético, como podemos observar nas distribuições eletrônicas a seguir:
→ Cobre:
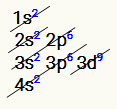
O cobre possui o subnível 3d9 como o mais energético em sua distribuição
→ Platina:

A platina possui o subnível 5d8 como o mais energético em sua distribuição
→ Paládio:

O paládio possui o subnível 4d8 como o mais energético em sua distribuição
→ Mercúrio:

O mercúrio possui o subnível 5d10 como o mais energético em sua distribuição
→ Prata:
.jpg)
A prata possui o subnível 4d9 como o mais energético em sua distribuição
→ Ouro:

O ouro possui o subnível 5d9 como o mais energético em sua distribuição
Apresentação física
Quanto à coloração e estado físico (em temperatura ambiente), esses metais apresentam-se da seguinte forma:
-
Ouro: é um sólido de cor amarelada
-
Prata: é um sólido de cor prateada
-
Platina: é um sólido de cor prateada
-
Paládio: é um sólido de cor branca prateada
-
Cobre: é um sólido de cor avermelhada
-
Mercúrio: é um líquido de cor prateada
Solubilidade
-
Ouro: solúvel apenas no Mercúrio e na água-régia, a qual é uma mistura de ácido clorídrico (HCl) e ácido nítrico (HNO3);
-
Prata: Solúvel em ácido nítrico;
-
Platina: Não é solúvel em nenhum material;
-
Paládio: Solúvel em ácidos inorgânicos ou soluções com bases inorgânicas;
-
Cobre: Solúvel em ácidos inorgânicos;
-
Mercúrio: não é solúvel em nenhum material;
Temperaturas de fusão e ebulição
Todos os metais nobres, para terem seus estados físicos alterados, requerem elevadas temperaturas, como podemos observar abaixo:
-
Ouro: ponto de fusão igual a 1064oC e ponto de ebulição igual a 2970oC;
-
Prata: ponto de fusão igual a 960,8oC e ponto de ebulição igual a 2210oC;
-
Platina: ponto de fusão igual a 1769oC e ponto de ebulição igual a 3825oC;
-
Paládio: ponto de fusão igual a 1554oC e ponto de ebulição igual a 2963oC;
-
Cobre: ponto de fusão igual a 1085oC e ponto de ebulição igual a 2562oC.
O único metal nobre que foge à regra descrita acima é o mercúrio, que apresenta temperaturas de fusão e ebulição bem baixas em comparação com os outros:
-
Mercúrio: ponto de fusão igual a -38,8oC e ponto de ebulição igual a 356,7oC.
Formas de obtenção
Os metais nobres, de uma forma geral, são encontrados em minérios e associados a outros materiais.
-
Ouro: Obtido, por exemplo, de forma livre na natureza ou no minério pirita;
-
Prata: obtida, por exemplo, no minério argentita;
-
Platina: Obtida, por exemplo, a partir do minério sperrilita;
-
Paládio: obtido, por exemplo, a partir de minérios de níquel;
-
Cobre: obtido, por exemplo, a partir do minério calcopirita;
-
Mercúrio: obtido, por exemplo, a partir do minério cinabre.
Utilizações
Alguns exemplos de utilizações dos metais nobres são:
-
Ouro: Produção de dispositivos de diagnóstico para gravidez e no tratamento do câncer;
-
Prata: produção de explosivos e baterias;
-
Platina: Produção de peças de reconstrução dentária e catalisadores de reações químicas;
-
Paládio: Produção de componentes eletrônicos e catalisadores para reações químicas;
-
Cobre: Produção de fios elétricos e geradores de energia;
-
Mercúrio: Produção de termômetros e soda cáustica.