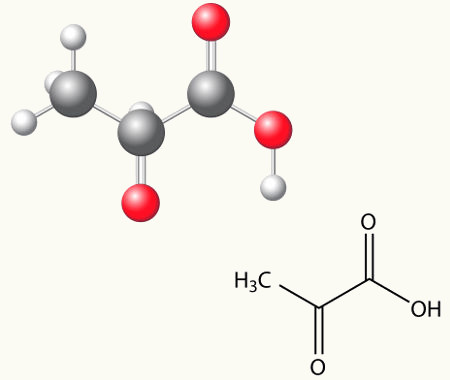
As reações de oxidação energética em aromáticos são fenômenos químicos que ocorrem quando esse grupo de compostos orgânicos é colocado em um meio que possui uma solução formada por água, ácido sulfúrico e permanganato de potássio (reagente de Bayer).
Veja a equação geral que representa os reagentes que participam de uma oxidação energética em aromáticos:
.jpg)
De forma geral, os produtos dessa reação são água, (H2O), gás carbônico (CO2) e um ácido carboxílico. Vale ressaltar que essa reação orgânica só ocorre quando há aromáticos que apresentam radicais alquila ligados a eles.
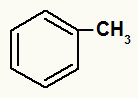
O radical metil é um exemplo de radical alquila
Reagente de Baeyer
Quando o reagente de Baeyer (permanganato de potássio - KMnO4) é misturado com água e ácido sulfúrico, temos a ocorrência de uma reação química. Veja:
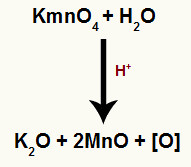
Equação química da reação com reagente de Baeyer em meio ácido
Nessa reação, temos a formação do óxido de manganês II (MnO), óxido de potássio (K2O) e oxigênios nascentes – estes são os responsáveis pela oxidação do aromático.
Princípios de uma oxidação energética em aromáticos
-
1º Princípio: o ataque ao aromático é realizado por oxigênios nascentes provenientes da solução com o reagente de Bayer. Esse ataque rompe, por exemplo, a ligação sigma entre os carbonos do radical do aromático.
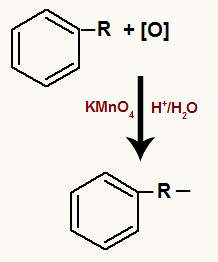
Rompimento de ligação sigma na ramificação do aromático
OBS.: Caso a ramificação ligada ao aromático tenha mais de um carbono, cada ligação sigma será rompida em virtude do ataque dos oxigênios nascentes.
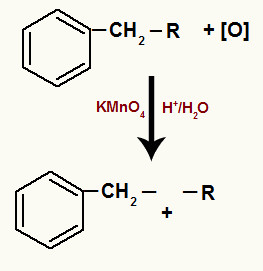
Rompimento das ligações sigmas entre os carbonos do radical do aromático
-
2º Princípio: cada valência criada pela quebra das ligações sigma é ocupada por um grupo hidroxila (resultante da união de um oxigênio nascente e um hidrônio proveniente da água).
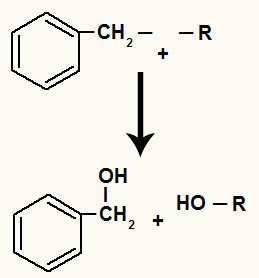
Hidroxilas ligadas aos carbonos que apresentavam valência livre
-
3º Princípio: cada um dos hidrogênios pertencentes aos carbonos do radical ligado ao aromático une-se a um oxigênio nascente.
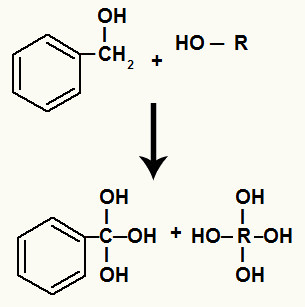
Ligação de oxigênios nascentes nos hidrogênios dos carbonos do radical
-
4º Princípio: uma estrutura que apresenta duas ou mais hidroxilas ligadas a um carbono é instável, por isso, ocorre a formação de uma molécula de água a cada duas hidroxilas ligadas a um mesmo carbono.
Não pare agora... Tem mais depois da publicidade ;)
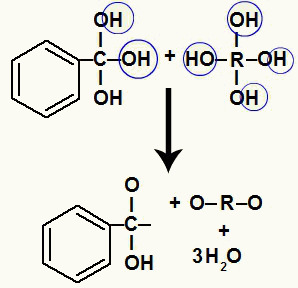
Formação de moléculas de água a partir das hidroxilas presentes nas estruturas
-
5º Princípio: entre o carbono e o oxigênio restante da hidroxila, há uma ligação sigma. Após a formação das moléculas de água, ocorre a formação de uma ligação pi entre eles.
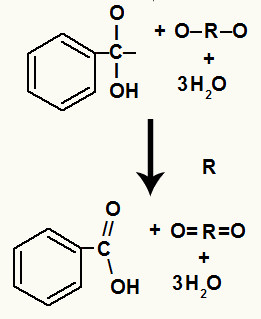
Formação de uma ligação pi entre o carbono e o oxigênio
Exemplo de uma reação de oxidação energética em aromáticos
Como exemplo, vamos mostrar a oxidação energética do etilbenzeno.
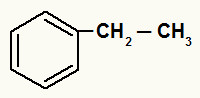
Fórmula estrutural do etilbenzeno
Quando o etilbenzeno é colocado em uma solução aquosa ácida (H2O com ácido sulfúrico) que possui reagente de Baeyer (KMnO4), os oxigênios nascentes ([O]) formados a partir do reagente de Baeyer atacam a molécula orgânica, quebrando a ligação sigma entre os carbonos do etil, o que forma uma valência livre em cada um deles.
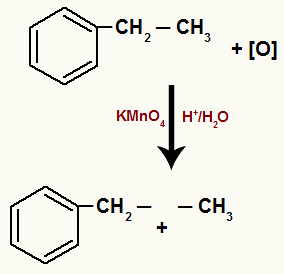
Quebra da ligação sigam nos carbonos do etil
Logo em seguida, cada valência livre formada na quebra da ligação sigma é preenchida por uma hidroxila (resultante da união de um oxigênio nascente e um hidrônio).
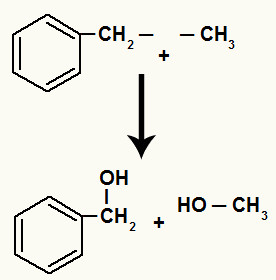
Hidroxilas nos carbonos que tiveram a ligação sigma entre eles rompida
Além disso, cada hidrogênio ligado aos carbonos que tiveram a ligação sigma rompida liga-se a um oxigênio nascente, formando a hidroxila.
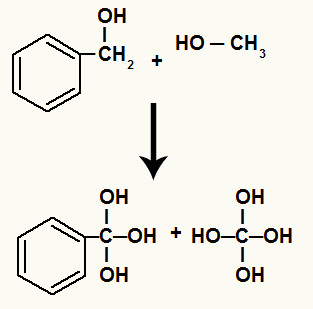
Ligação de oxigênios nascentes nos hidrogênios dos carbonos envolvidos na quebra
Como temos várias hidroxilas em um mesmo átomo de carbono, forma-se uma estrutura instável. Por essa razão, ocorre a decomposição dessas hidroxilas, de forma que, a cada duas hidroxilas, forma-se uma molécula de água.
.jpg)
Formação de moléculas de água a partir das hidroxilas em carbono instável
Após a decomposição das hidroxilas, temos a formação de uma ligação pi.
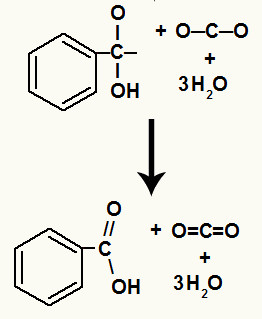
O ácido carboxílico originado nessa reação foi o ácido benzoico.