No texto Distribuição Eletrônica foi explicado como é realizada a distribuição eletrônica dos elementos no diagrama de energia de Pauling. Por meio dessa distribuição eletrônica é possível saber a família e o período do elemento na Tabela Periódica.
Fazendo a distribuição dos elétrons de todos os elementos, o último subnível eletrônico encontrado para cada um deles foi o mostrado na Tabela abaixo:
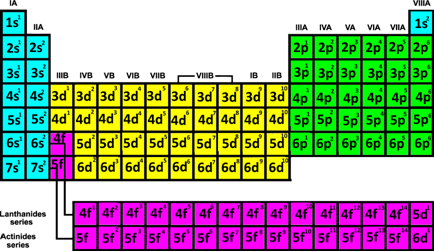
Note que existe uma ordem nessas distribuições. Vejamos como podemos identificar os períodos dos elementos:
- Períodos: Correspondem às sete linhas horizontais que aparecem na tabela.
Observe na tabela acima que os dois elementos do primeiro período ou primeira linha (H e He, em azul) possuem a camada 1, que é a K, na sua distribuição eletrônica. Já os do segundo período possuem a camada 2, que é a L, e os do terceiro possuem o nível de energia igual a 3, que é o M, e assim por diante. Portanto, podemos chegar à seguinte conclusão:
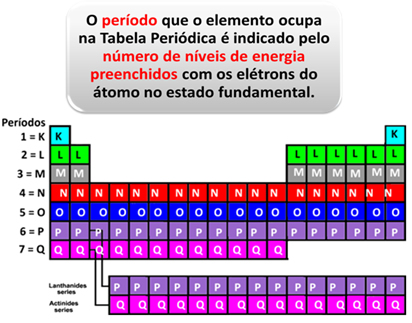
Por exemplo, vamos fazer a distribuição eletrônica do oxigênio (8O), do ferro (26Fe) e do iodo (53I). O último subnível preenchido está em destaque:
8O: 26Fe: 53I:
K 1s2 K 1s2 K 1s2
L 2s2 2p4 L 2s2 2p6 L 2s2 2p6
M 3s 3p 3d M 3s2 3p6 3d3 M 3s2 3p6 3d10
N 4s 4p 4d 4f N 4s2 4p 4d 4f N 4s2 4p6 4d10 4f
O 5s 5p 5d 5f O 5s 5p 5d 5f O 5s2 5p5 5d 5f
P 6s 6p 6d P 6s 6p 6d P 6s 6p 6d
Q 7s 7p Q 7s 7p Q 7s 7p
O oxigênio está no segundo período porque ele possui duas camadas eletrônicas (K e L); o ferro está no quarto período porque ele possui quatro camadas eletrônicas (K, L, M e N), e o iodo está no quinto período da Tabela Periódica porque ele possui cinco camadas eletrônicas (K, L, M, N e O).
Veja como isso é verdade:
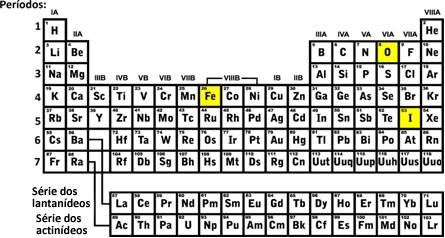
Agora, consideremos como a distribuição eletrônica nos indica a família do elemento na Tabela Periódica:
- Família ou grupos: São as 18 colunas que aparecem na Tabela.
Voltando na primeira tabela que mostramos nesse texto, podemos observar que na distribuição eletrônica de todos os elementos da família 1A o último subnível a ser preenchido é o s com apenas um elétron. Já os da família 2A terminam todos com o subnível s preenchido com dois elétrons, e assim sucessivamente:
- Família 3A: Todos possuem 3 elétrons no último nível e a configuração eletrônica termina em ns2 np1;
- Família 4A: Todos possuem 4 elétrons no último nível e a configuração eletrônica termina em ns2 np2;
- Família 5A: Todos possuem 5 elétrons no último nível e a configuração eletrônica termina em ns2 np3;
- Família 6A: Todos possuem 6 elétrons no último nível e a configuração eletrônica termina em ns2 np4;
- Família 7A: Todos possuem 7 elétrons no último nível e a configuração eletrônica termina em ns2 np5.
Desse modo, podemos concluir o seguinte:

No caso dos elementos representativos (1, 2, 13, 14, 15, 16, 17 e 18) ou dos elementos que estão nas colunas A (IA, IIA, IIIA, IVA, VA, VIA, VIIA, VIII A), temos que o seu elétron mais energético estará sempre no subnível s ou p.
Exemplos:
11Na: 17Cl:
K 1s2 K 1s2
L 2s2 2p6 L 2s2 2p6
M 3s1 3p 3d M 3s2 3p5 3d
N 4s 4p 4d 4f N 4s 4p 4d 4f
O 5s 5p 5d 5f O 5s 5p 5d 5f
P 6s 6p 6d P 6s 6p 6d
Q 7s 7p Q 7s 7p
O sódio (Na) é da família 1A porque há apenas 1 elétron na sua última camada eletrônica, e o cloro (Cl) é da família 7A porque ele possui sete elétrons na última camada (2 + 5). Ambos são elementos representativos, porque o último subnível do sódio é o s e o do cloro é o p.
.jpg)
Os elementos de transição são aqueles pertencentes às famílias de 3 a 12 ou que estão nas colunas B (3 B, 4 B, 5B, 6B, 7B, 8B, 1B e 2B). Eles são classificados em elementos de transição externa e interna. Veja como descobrir à qual desses grupos o elemento pertence por meio da sua distribuição eletrônica:
- Elementos de transição externa: O último elétron a ser preenchido se situa em um subnível d incompleto, ou seja, a sua configuração eletrônica termina em (n-1)d (1 até 8).
Exemplos:
74W: 28Ni:
K 1s2 K 1s2
L 2s2 2p6 L 2s2 2p6
M 3s2 3p6 3d10 M 3s2 3p6 3d8
N 4s2 4p6 4d10 4f10 N 4s2 4p 4d 4f
O 5s2 5p6 5d8 5f O 5s 5p 5d 5f
P 6s2 6p 6d P 6s 6p 6d
Q 7s 7p Q 7s 7p
O último subnível do tungstênio (W) que foi preenchido foi o 5d8 e o do níquel (Ni) foi o 3d8, isso quer dizer que eles são elementos de transição externa, veja:
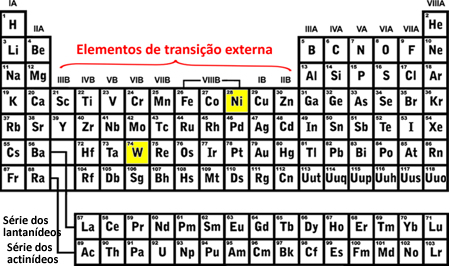
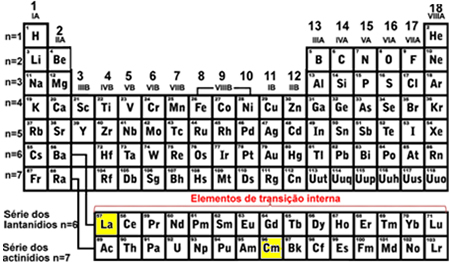
- Elementos de transição interna: são os elementos da série dos lantanídeos e dos actinídeos. O último elétron a ser preenchido se situa em um subnível f incompleto, ou seja, a sua configuração eletrônica termina em (n - 2)f (1 até 13).
Exemplos:
57La: 96Cm:
K 1s2 K 1s2
L 2s2 2p6 L 2s2 2p6
M 3s2 3p6 3d10 M 3s2 3p6 3d10
N 4s2 4p6 4d10 4f1 N 4s2 4p6 4d10 4f14
O 5s2 5p6 5d 5f O 5s2 5p6 5d10 5f8
P 6s2 6p 6d P 6s2 6p6 6d
Q 7s 7p Q 7s2 7p
O último subnível a ser preenchido do lantânio (La) foi o 4f1 e do Cúrio (Cm) foi o 5f8, ambos com o subnível f incompleto, indicando que eles são elementos de transição interna:
Videoaula relacionada: